

Extra Quality
これまでの伝統を受け継ぎながらも、社会の変化に対応した進歩を続ける日本医科大学。その源となっている教育や研究についてご紹介します。
ビリビリとした痛み治療の鍵は小さな粒子「個の医療」見据えて
hippocrates 29号 2026年04月発行
-
神経が傷ついて起きる、しびれに似た痛み。厄介なこの痛みの効果的治療を目指して、日本医科大学医学部薬理学の坂井敦先生は、私たちの体内に存在する「細胞外小胞」と呼ばれる微小粒子に着目し、研究を進めています。その患者の痛みの慢性化リスクの指標となるバイオマーカーの候補を細胞外小胞に含まれる物質から見出したほか、放出される細胞外小胞の量が痛みの発生・悪化に関わることを解き明かしています。見据えているのは「個々の患者に合った痛み治療」の確立です。
体で感じる痛みには、「ビリビリ」「チクチク」「ジンジン」などと表現されるタイプがあります。しびれにも似たこのタイプの痛みは、体の感覚神経が障害されて起きることから「神経障害性疼痛(とう つう)」といいます。原因は、がんによる神経の圧迫、抗がん剤の副作用のほか、糖尿病、帯状疱疹、坐骨神経痛、外傷によるものなどさまざまです。他のタイプの痛みと違って一般的な鎮痛薬ではおさまりにくく、効果的な治療法の出現が期待されています。
-

「必要のない痛みをなくすことが何よりの目標です。簡単ではありませんが、貢献できたらと思っています」
こう話すのは、日本医科大学医学部薬理学准教授の坂井敦先生です。神経障害性疼痛のより効果的な治療に向け、研究を進めています。
細胞外小胞に痛み治療の鍵を見出す
坂井先生が着目しているのが、私たちの体内に無数に存在する「細胞外小胞」という粒子です。これは名前の通り、細胞の外へと放出されるナノメートル単位の小さな膜性の粒子。膜で覆った中にタンパク質やリボ核酸(RNA)など多様な物質を収めています。
細胞外小胞に着目した理由について、坂井先生は「その患者さんの痛みの特徴やリスクを知るための指標であるバイオマーカーの候補が、細胞外小胞の中に存在していることがわかったからです」と説明します。
そのバイオマーカーの候補とは「長鎖非コードRNA」と呼ばれるRNAの一種。細胞外小胞の中に入って細胞外へと放たれます。坂井先生ら研究チームは、長鎖非コードRNAのいくつかの種類が、その患者の神経障害性疼痛の「慢性化リスク」を知るバイオマーカーになりうることを見出しました。研究では、抗がん剤の一つ、オキサリプラチンの副作用としての痛みを対象として、細胞外小胞の中の長鎖非コードRNAを網羅的に解析することでマーカー候補を定めることができました。
「患者さんの血中に含まれる特定の長鎖非コードRNAの量が増えないほど、生じた痛みが慢性化するリスクが高いのです。その慢性化リスクが高いとわかった患者さんには、オキサリプラチンの使用量を減らしたり、他の抗がん剤に代えたり、治療法を工夫する余地が出てきます。同様のアプローチで、他の原因による痛みについても慢性化リスクなどのバイオマーカーを確立できる可能性があると思っています」
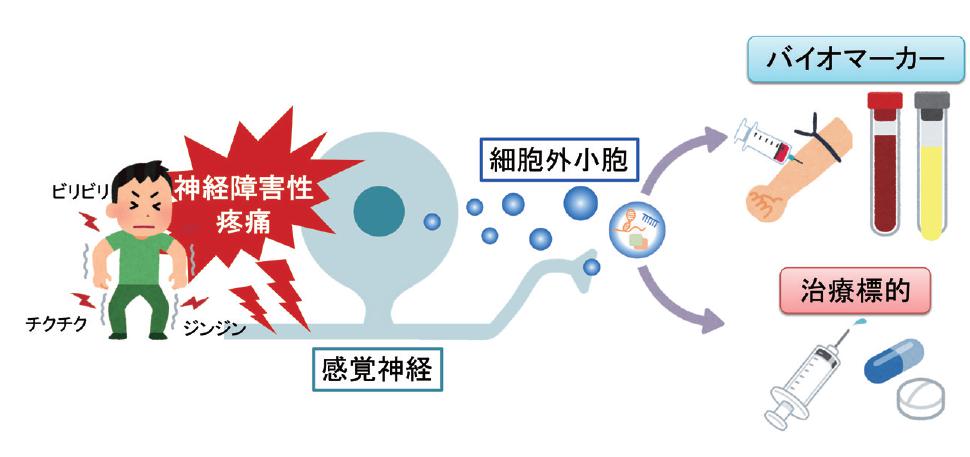
神経障害生疼痛の効果的な治療に向けた研究。細胞外小胞を起点に、新たなバイオマーカーや治療標的を見出している
ビリビリのメカニズムも研究
先に見据えるのは個別化医療
細胞外小胞に着目して研究している坂井先生は、神経障害性疼痛のバイオマーカーを見出しただけでなく、発症メカニズムの解明にも挑んでいます。
「バイオマーカーの研究を進める中で、細胞外小胞の放出量を決めるのはどういうものなのだろうかという問いが生じました。この問いが転じて、神経障害性疼痛では放出される細胞外小胞の量そのものが増えるというメカニズムが見えてきました」
神経障害疼痛が生じる流れを見ていくと、まず体の末梢の感覚神経で、神経栄養因子と呼ばれるタンパク質の一種が細胞外小胞の放出量を増やす。細胞外小胞の放出量が増えると、マクロファージという免疫細胞の一種が神経で炎症をもたらす。これで神経が障害を受け、痛みが生じる、という経路です。
以前から神経栄養因子の活性化が痛みにつながることは知られていましたが、坂井先生は新たに、その途中で「細胞外小胞の放出が促進されている」ことを解き明かしました。
痛み発生の経路を知ることは、痛みの治療標的を視界に収めることを意味します。「途中の細胞外小胞の放出をブロックするという治療法は考えられます。ただし、具体的にどうブロックするかはまだ難問です。細胞外小胞そのものにも未解明な点が多くあります。今後の細胞外小胞の研究の進展とマッチしていけば、治療法につなげられるかもしれません」。
その先に見据えているのは、これらの成果を組み合わせた個別化医療です。
-
「例えば、バイオマーカーで患者さんたちの痛みの特徴を層別化し、特徴ごとに患者さんに効果的な治療薬を投与するといったイメージです。細胞外小胞を通じて、バイオマーカーと治療法のリンクができはじめました」
未来社会では、がんなどの病気の治療法が進歩し、病気経験者がより長く生きつづけられると期待されています。同時に、手術痕の影響や継続服用薬の副作用など、治療後の痛みと長くつきあっていく人も増えるでしょう。痛み治療の重要性は一層高まりそうです。「患者さんたちの利益につながる研究を意識しながら、自分たちの強みを治療につなげようとしています」
-

日本医科大学大学院医学研究科薬理学分野の研究室のメンバーたち。研究室には博士課程大学院生も多数在籍。坂井先生は医学部3年生の研究配属での指導も務める

坂井 敦先生(さかい・あつし)
日本医科大学
医学部 医学科 薬理学
准教授
2004年東京医科歯科大学大学院保健衛生学研究科博士(前期)課程修了。2010年日本医科大学大学院博士号(医学)取得。この間、同大学医学部薬理学助手、同助教。同講師を経て2024年より現職。学内研究者の活動活性化や成果活用促進を支えるURA※を兼任。
※University Research Administrator


