

Extra Quality
炎症のしくみに重要なインフラマソーム形成
その”前段“から解明
hippocrates 17号 2023年04月発行

炎症反応は、主に自然免疫細胞のマクロファージが炎症性サイトカインをつくり出すことで生じます。日本医科大学大学院医学研究科微生物学・免疫学大学院教授の森田林平先生は、この炎症反応における主要な分子複合体インフラマソームの構成分子の一つであるNLRP3のインフラマソーム形成前の“在り方”からアプローチすることにより、各種の細胞内小器官におけるNLRP3インフラマソーム形成制御のしくみを解明しようとしています。
発赤・はれ・熱・痛みなどとして現れる「炎症」。なかでも急性炎症は、免疫細胞の一つであるマクロファージが、インターロイキン1β(IL–1β)やIL–6、また腫瘍壊死因子(TNF–α)などの炎症性サイトカインをつくり出すことにより生じます。
炎症性サイトカインのなかでも、IL–1βは、IL–6やTNF–αなどと違ってマクロファージを刺激してもつくられにくく、別のしくみでつくり出されると考えられてきました。このIL–1β産生のしくみに必須であるのがcaspase–1という酵素の活性化です。
とはいえ、caspase–1が活性化する分子機序は20世紀において未解明でした。これに対し2002年、caspase–1の活性化は、caspase–1自体と、ASCやNLRP3からなる分子複合体の形成により起きることが、スイスの免疫学者ユルグ・チョップによって解明され、この複合体は「インフラマソーム」と命名されました。
インフラマソームが発見されて以降、IL–1βがつくられるしくみがわかったことで、炎症性疾患の病態解明などが進みました。NLRP3インフラマソーム形成の誘導物質としてアデノシン三リン酸(ATP)や細菌毒素ニゲリシン、また、アスベスト、コレステロール結晶、尿酸ナトリウム結晶が同定されています。
こうしたなか、インフラマソームの構成タンパク質の一つであるNLRP3に着目し、「NLPR3がインフラマソームを形成する前に、どのような状態で細胞内に存在しているのか」をテーマに研究しているのが森田林平先生です。
インフラマソーム形成前に着目
NLRP3はどんな状態にあるか
森田先生は2008年6月、博士研究者(ポスドク)として米国イェール大学の免疫学者リチャード・フラヴェルの研究室に入り、インフラマソームの研究に取り組むよう言われました。「実は、それまでインフラマソームを知らなかったのですが、ラボの同僚の女性研究者が親切に研究の意義や手法を教えてくれたのです。そこで私は、極めて厳格で洗練されたしくみにより炎症反応が制御されているのだと知り、驚きとともにインフラマソームに強い興味をもつようになりました」
森田先生は、インフラマソーム形成の未解明な部分に光を当てるべく研究を行っています。数多くのインフラマソーム研究者がいるなか、自身の研究の独自性を見出すべく、そもそも構成タンパク質のNLRP3がどのような状態にあるかを解明することにしたのです。「私が知る限り、インフラマソーム形成前の分子状態からアプローチをする研究者は当時いませんでした」
森田先生は、NLRP3に結合するタンパク質を同定していきました。すると、それらのタンパク質の分子は、細胞内小器官などの分子と密接にかかわっていることがわかってきたのです。たとえば、ミトコンドリア、ゴルジ体、小胞体、それにエンドソームといった細胞内小器官(オルガネラ)や細胞骨格です。
「これらのことから今考えているのは、NLRP3は特定の場所に存在するのでなく、ミトコンドリア、小胞体、エンドソームなどに分かれて存在し、刺激によりそれぞれの細胞内小器官にてつくられるということ。NLRP3の出どころは一つではないと見ています」
-
いま森田先生がとくに着目しているのが、エンドソームとNLRP3の関係性です。エンドソームは、細胞のエンドサイトーシス(飲食作用)によって細胞内に取り込まれた物質を輸送・代謝するのに関与する袋状の構造体。「エンドサイトーシスによるエンドソームの形成は、ほぼあらゆる細胞で当たり前に起きるものですが、これがNLRP3に関与し、インフラマソームの形成を制御していると見ています。このような当たり前の細胞の営みが、炎症を制御していることを解明したい」
-
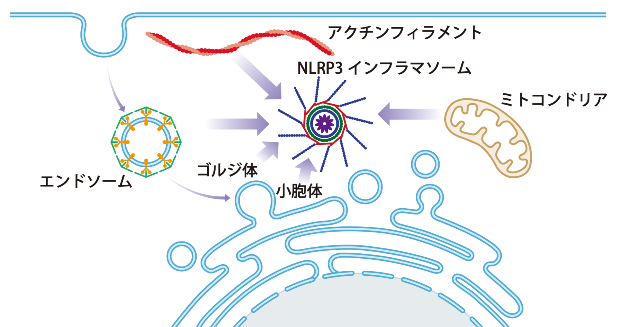
NLRP3はミトコンドリア、小胞体、エンドソームなどに存在し、刺激によりそれぞれの細胞内小器官で活性化し、その後インフラマソームを形成すると考えられる
「炎症によるがん免疫療法」の実現も視野に入れて研究
さらに森田先生は、インフラソーム形成による炎症が、がんの成長の抑制に関与していると見て、「炎症によるがん免疫療法」の実現も視野に入れています。NLRP3に結合する分子のなかに、がん細胞の死を誘導する分子があることも見出したのです。「インフラマソームが炎症性サイトカインをつくる一連のしくみは自然免疫におけるもの。今後は、がん治療への応用に向け、獲得免疫とのつながりも解明していければと考えています」
-
ただし、自身の研究がどう進んでいくか、さまざまな選択肢がありうるとも言います。「研究室の大学院生たちと研究論文の精読会や研究の進捗報告会をしているなかで、私自身おもしろいと感じる発想や報告を得たりもします。若い人たちから刺激を受けながらの日々ですから、5年後はまったく異なる研究をしているかもしれません」 新たなことに貪欲でありながら研究を進めていく姿勢です。
-

ラボのメンバーたちと

森田 林平 先生(もりた・りんぺい)
日本医科大学大学院医学研究科微生物学・免疫学教室
大学院教授
2002年に京都大学大学院医学研究科血液・腫瘍内科学修了。博士(医学)。米ベイラー免疫学研究所ポスドク、米イェール大学フラヴェル研究室ポスドク、慶應義塾大学医学部微生物学・免疫学准教授、国際医療福祉大学医学部免疫学教授を経て、2019年より現職。


