

Extra Quality
分子レベルで病態解明
非アルコール性脂肪肝炎の
治療法開発を目指す
hippocrates 10号 2021年08月発行

脂肪肝から肝炎、肝硬変へと進行する可能性のある非アルコール性脂肪性肝疾患(NAFLD)の推定有病率は、世界で25・2%に上ります。中でも炎症と線維化が特徴の非アルコール性脂肪性肝炎(NASH)は、有力な治療法がまだなく、大きな問題です。日本医科大学大学院医学研究科大学院教授の酒井真志人先生は、肝臓の中にあるマクロファージの分化に関する研究を通じて、NASHの分子レベルでの病態解明に迫っています。
肝臓マクロファージを研究の対象に選ぶ
多様な機能を持つ肝臓は、細胞の種類も多彩で、肝細胞(肝実質細胞)以外にも、類洞内皮細胞、肝星細胞、白血球の一種であるマクロファージなど、さまざまな細胞が存在し、それぞれが協調して機能を発揮しています。酒井真志人先生は、肝臓マクロファージを自身の研究テーマに選びました。
「テーマに選んだ理由は3つ。マクロファージは全ての臓器に存在していますが、各臓器で働きが異なります。しかし、肝臓のどのようなシグナルが肝臓特有のマクロファージを作るのか、これまで分かっていませんでした。それが1つ目です。2つ目は、肝臓マクロファージはNASHにおける炎症や線維化の促進に関係すると考えられ、NASHの病態の解明という意味でも重要だからです。そして3つ目は、もともと肝細胞における糖・脂質代謝の研究をしていたので、肝臓内にある免疫細胞も研究して、代謝調節における、それらの細胞同士の相互作用の役割を調べたいと考えたからです」
肝臓の常在性マクロファージとしては、類洞内皮細胞上にくっつくように存在している「クッパー細胞」が知られています。クッパー細胞はマクロファージの一種で、自然免疫や鉄代謝に重要な役割を果たしています。
このクッパー細胞は、肝臓が健康な状態の時には、自ら分裂を繰り返すことにより維持されています。しかし、感染症やNASHのような病的な状態において、クッパー細胞の細胞死が起こり類洞から取り除かれると、血液中の単球が肝臓に遊走し、肝臓内でクッパー細胞のような肝臓マクロファージに分化するのです。
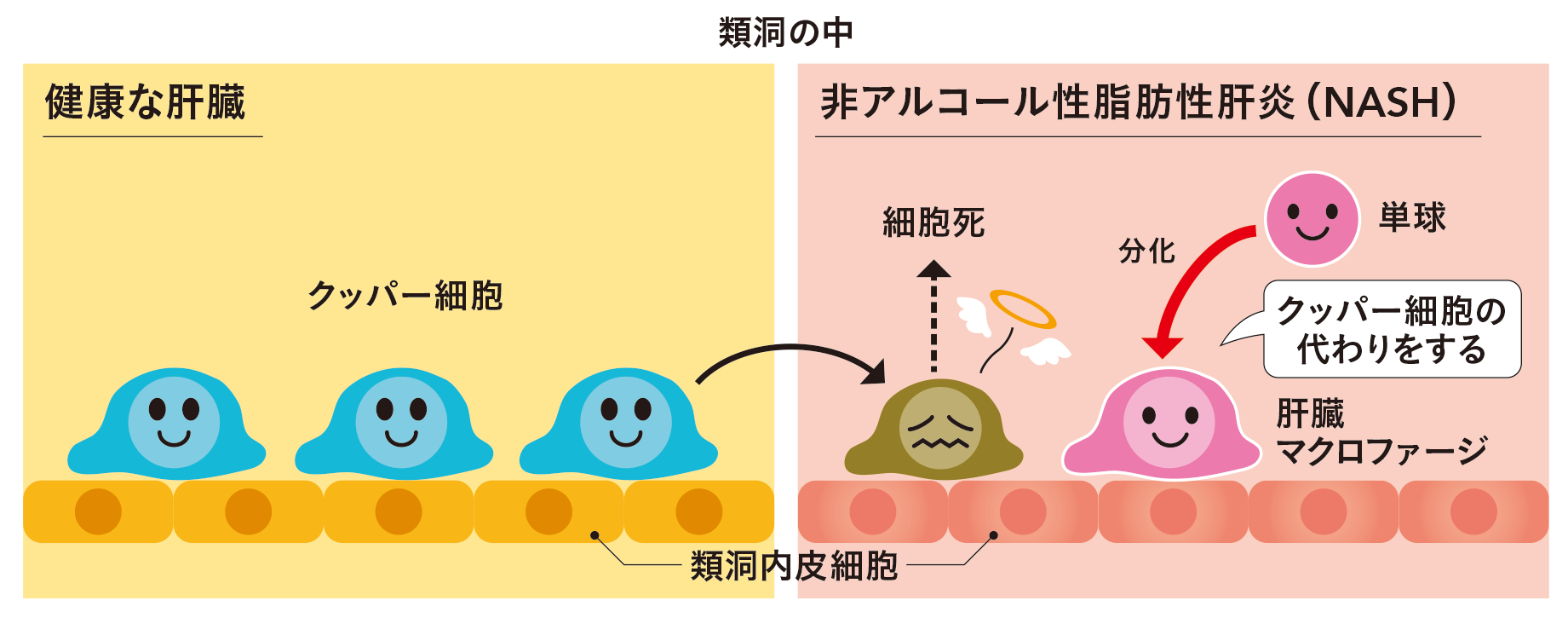
単球が分化してクッパー細胞の代わりをする
血液中の単球が肝臓マクロファージに分化
酒井先生たちは、この現象を利用して、単球が肝臓マクロファージに分化する過程を観察することで、肝臓マクロファージの分化に必要なシグナルを同定しました。マウスを使った実験で、肝臓に遊走した単球の変化を日を追って調べることにより、もともと単球だった細胞の遺伝子発現が、次第にクッパー細胞の遺伝子発現に近づくことを確認しました。
細胞はみな同じDNAを持っているのに、発現する遺伝子と発現しない遺伝子があるのは、DNA上のエンハンサーという部分で、その発現がコントロールされているからです。酒井先生は、分化途上にある肝臓マクロファージのエンハンサー上で転写因子が結合するDNA配列を調べ、分化のスイッチを入れる3種類のシグナルを突き止めることに成功しました。
肝臓の中の類洞という微小な環境に単球が定着したときに、これらのシグナルが活性化し、単球が肝臓マクロファージへと分化していくのです。こうしてできた単球由来の肝臓マクロファージは、NASHにおける炎症・線維化に関係していると考えられています。
「単球が肝臓に遊走することを抑制する薬剤も開発されています。ただ、単球が肝臓マクロファージに分化することには、失われたクッパー細胞を補っているというプラスの側面もあるはずです。NASHの治療法は、単に単球の遊走を抑制するというより、多様な肝臓マクロファージの働きを深く理解した上で考えていく必要があります」
NASHの肝臓には4種類のマクロファージが存在
酒井先生は、NASHの肝臓に存在するマクロファージについて、考えられるあらゆる手法を駆使して検討しました。その結果、NASHの肝臓には、もともとあるクッパー細胞を含めて計4種類のマクロファージが存在することを突き止め、それぞれが存在する場所を特定しました。単球が類洞に遊走すると、先に述べたメカニズムでクッパー細胞のようなマクロファージに分化しますが、同じ単球でも血管の周囲に遊走したものは、異なる性質を持つマクロファージに分化していたのです。
「肝硬変を起こした肝臓には『瘢痕随伴マクロファージ』があり、これが線維化を促進するといわれています。実はNASHでも、瘢痕随伴マクロファージの存在を示すマーカーが上昇していることが分かっています。一方、肝臓の線維化の修復過程でマクロファージを除去すると、逆に治りが悪くなることが知られています」
肝臓マクロファージには、肝臓の線維化を促進する働きと、線維化を改善する働きの両方があることが分かりました。多様な肝臓マクロファージのそれぞれの特徴をさらに突き詰めることで、NASHの病態に迫ることができ、その治療法の開発にもつながるのではないかと酒井先生は考えています。

研究スタッフの面々

酒井 真志人先生(さかい・ましと)
日本医科大学大学院医学研究科 分子遺伝医学分野 大学院教授
2002年に神戸大学医学部を卒業後、神戸大学大学院、国立国際医療研究センター研究所で糖尿病の発症メカニズムを研究。2012年に博士号(医学)を取得。その後、同研究所分子代謝制御研究部室長を経て、2016年から2020年まで米国カリフォルニア大学サンディエゴ校に留学。2020年8月より現職。2021年度より科研費基盤研究(B)「肝臓の糖脂質代謝とNAFLDにおけるマクロファージ由来因子による転写制御の意義」研究代表者。


